식약처, 만성콩팥병 위험 평가 SW 등 2개 제품 지정
에이아이메딕 'HeartMedi', 메디웨일 'DrNoon CKD'
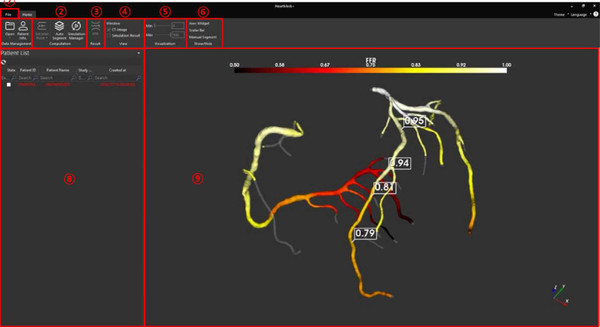
흉부 CT 영상으로 관상동맥의 협착정도를 평가하는 인공지능 기반 소프트웨이와 만성콩팥병 위험군을 대상으로 망막의 구조 및 망막 내 혈관모양을 분석해 만성콩팥병 발생 위험 정도를 표시하는 인공지능 기반의 소프트웨어가 혁신의료기기로 지정됐다.
식품의약품안전처는 22일 ㈜에이아이메딕이 개발한 관상동맥의 협착 정도를 평가하는 심혈관위험평가소프트웨어 'HeartMedi'와 ㈜메디웨일의 만성콩팥병 위험을 표시하는 병원진료용소프트웨어 'DrNoon CKD'를 제41호, 제42호 혁신의료기기로 지정했다고 밝혔다.
㈜에이아이메딕의 ‘HeartMedi’는 흉부 컴퓨터단층촬영(CT) 영상을 토대로 관상동맥을 3차원으로 형상화해 분획혈류예비력(FFR)을 전산유체역학(컴퓨터로 유체의 움직임을 모사해 수학적으로 예측) 기반으로 계산함으로써 관상동맥의 협착정도를 평가하는 국내 첫 제품으로, 통합심사‧평가에서 기술 혁신성 등을 인정받아 혁신의료기기로 지정됐다.
분획혈류예비력(Fractional Flow Reserve)은 관상동맥 협착부위에서 가까운 부위와 먼 부위에 있는 정상혈관의 각각 최대 혈류량을 비율(0~1)로 표현, 낮을수록 혈관 내 협착이 심한 것이다.
또 ㈜메디웨일의 ‘DrNoon CKD’는 인공지능으로 망막사진에서 망막의 구조와 망막 내 혈관모양을 분석해 만성콩팥병의 발생 위험정도를 저위험, 중증도위험, 고위험으로 평가해주는 국내 첫 제품으로, 일반심사에서 기술혁신성 등을 인정받아 혁신의료기기로 지정됐다.
현재 표준검사법은 혈액검사를 토대로 사구체여과율을 확인하는 방법을 사용하고 있으나, ‘DrNoon CKD’ 제품의 경우 망막혈관 이상과 만성콩팥병증 위험도가 밀접하다는 연구결과를 토대로 망막 사진에서 미세한 혈관 변화를 분석해 콩팥질환 발생을 예측한다.
통합심사·평가를 거쳐 혁신의료기기로 지정된 ‘HeartMedi’는 현재 품목허가를 신청해 심사 중인 제품으로, 향후 품목허가 완료 시 신의료기술평가위원회와 '신의료기술의 안전성·유효성 평가결과' 고시 개정·공포(30일)를 거쳐 비급여로 의료현장에 바로 진입해 3~5년간 사용될 예정이다.
아울러 일반심사를 거쳐 혁신의료기기로 지정된 ‘DrNoon CKD’는 현재 개발 중인 제품으로 향후 우선심사 등 허가심사 특례를 적용받을 수 있어 신속한 제품화에 도움이 될 것으로 기대된다.
식약처 의료기기안전국 관계자는 "현재까지 총 42개 제품을 혁신의료기기로 지정했으며, 이러한 혁신의료기기 지정 제도 운영은 정부 국정 과제인 ‘바이오·디지털헬스 글로벌 중심국가 도약’ 실현에 기여할 것으로 기대한다"고 말했다.
이어 "앞으로도 식약처는 앞으로도 식약처는 혁신의료기기가 의료현장에서 널리 사용될 수 있고 국민에게 안전하고 새로운 치료 기술을 신속히 제공하도록 혁신의료기기 제도를 효과적으로 운영하고 국민에게 안전하고 새로운 치료 기술을 제공하도록 노력하겠다"고 덧붙였다.

